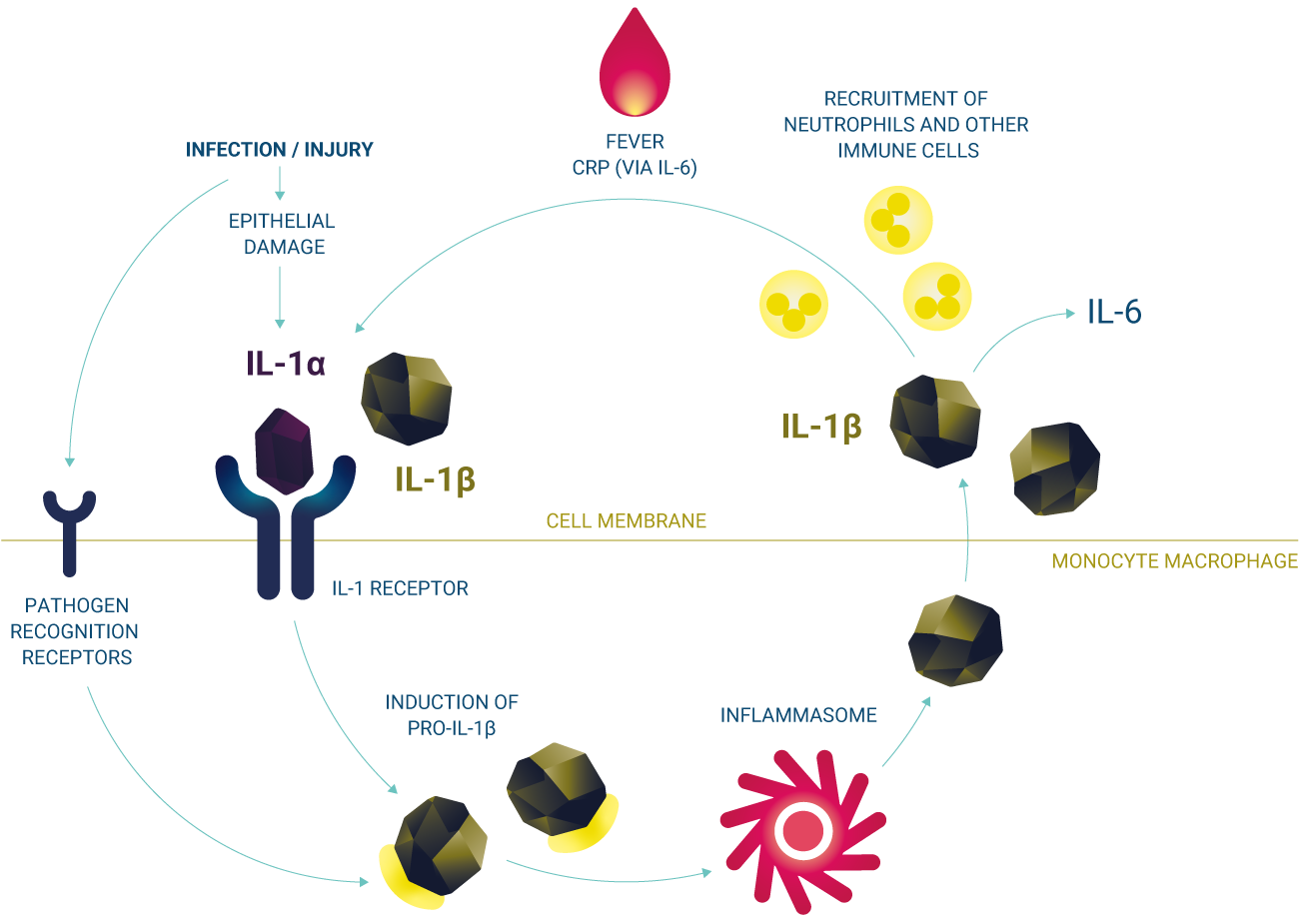
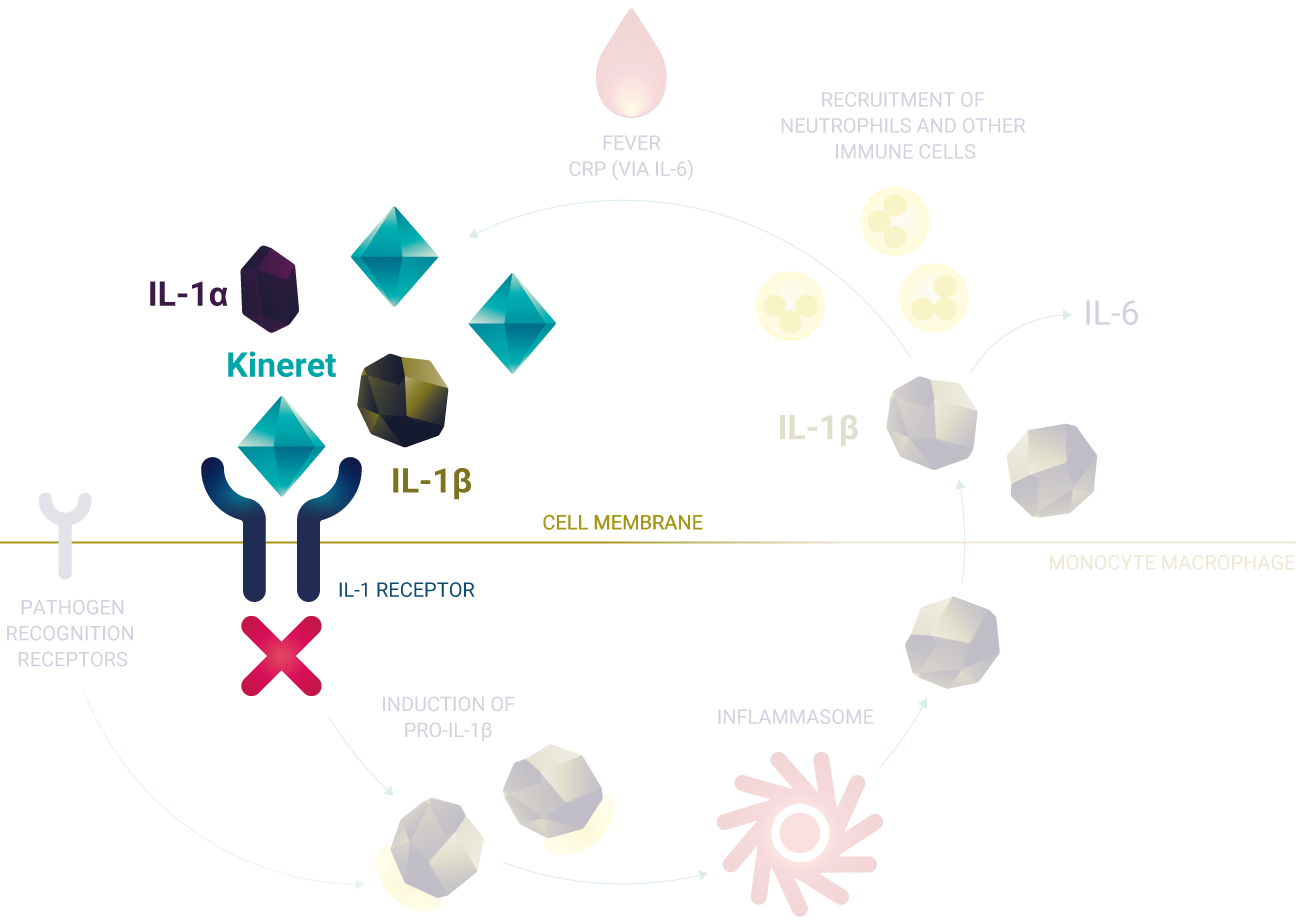
MODE OF ACTION
Kineret is a targeted treatment that neutralises the biological activity of both IL-1α and IL-1β1
Kineret is a recombinant version of the naturally occurring IL-1 receptor antagonist (IL-1Ra). Kineret acts by competitively inhibiting the biological activity of interleukin- 1α (IL-1α) and interleukin-1β (IL-1β), preventing both cytokines from attaching to the IL-1 receptor (IL-1R1) and initiating downstream signalling cascades.1,2 By blocking the interaction between IL-1α/IL-1β and IL-1R1, Kineret interrupts IL- 1-mediated inflammatory processes and alleviates the signs and symptoms of conditions characterised by excessive or dysregulated IL-1 responses.2
Approved indications for Kineret1
Rheumatoid Arthritis (RA) In adults for the treatment of the signs and symptoms of RA in combination with methotrexate, with an inadequate response to methotrexate alone.
COVID-19 Treatment of COVID-19 in adult patients with pneumonia requiring supplemental oxygen (low- or high-flow oxygen).
Cryopyrin-Associated Periodic Syndromes (CAPS) Neonatal-Onset Multisystem Inflammatory Disease (NOMID) / Chronic Infantile Neurological, Cutaneous, Articular Syndrome (CINCA) - Muckle-Wells Syndrome (MWS) and Familial Cold Autoinflammatory Syndrome (FCAS)
Familial Mediterranean Fever (FMF) Kineret should be given in combination with colchicine, if appropriate.
Still’s Disease Adults, adolescents, children and infants aged 8 months and older with a body weight of 10 kg or above for the treatment of Still’s disease, including Systemic Juvenile Idiopathic Arthritis (SJIA) and Adult-Onset Still’s Disease (AOSD).1
See Kineret Prescribing information for summary of product characteristics for full prescribing and safety information
FAST ONSET
This is fast onset and short half life
Kineret has high absolute bioavailability after subcutaneous administration; maxi- mum plasma concentrations are reached within 3 to 7 hours and the terminal eli- mination half-life is 4 to 6 hours. Kineret induces a rapid resolution of systemic features such as fever, rash, and elevation of acute phase reactants.1
Safety
Please refer to current SmPC for more information about the safety and efficacy of Kineret.
How is Kineret administered?
- Kineret is given in a pre-filled syringe containing 100 mg of anakinra per 0.67 ml (150 mg/ml).1
- Kineret is given once daily as a subcutaneous injection.1
- Dosage depends on indication. In children, the dose is determined depending on body weight. Please refer to current SmPC.
How should Kineret be stored?
- Kineret should be stored in a refrigerator between 2°C and 8°C.1
- Kineret should not be frozen or shaken.1
- Kineret should be kept in its original carton and away from light.1
Kineret, Rx, F (anakinra)
ATC kod: L04AC03. Immunsuppressiva medel, interleukinhämmare.
Indikationer: Reumatoid artrit (RA). Kineret är avsett att användas i kombination med metotrexat för behandling av symtom hos vuxna med RA som svarar otillräckligt på behandling med enbart metotrexat. Covid-19: Kineret är avsett för behandling av coronavirussjukdom 2019 (covid-19) hos vuxna patienter med pneumoni som behöver kompletterande syrgasbehandling (syrgasbehandling med lågflöde eller högflöde) och som löper risk att progrediera till svår andningssvikt fastställd som plasmakoncentration av suPAR (soluble urokinase plasminogen activator receptor) ≥ 6 ng/ml (se avsnitt 4.2, 4.4 och 5.1).
Periodiska febersyndrom:
Kineret är avsett för behandling av följande autoinflammatoriska periodiska febersyndrom hos vuxna, ungdomar, barn och spädbarn som är 8 månader och äldre med en kroppsvikt på 10 kg eller mer.
Kryopyrinassocierade periodiska syndrom (CAPS) Kineret är avsett för behandling av CAPS, inklusive: -systemisk multiinflammatorisk sjukdom med neonatal debut (NOMID)/kroniskt infantilt neurologiskt hud- och ledsyndrom (CINCA) -Muckle-Wells syndrom (MWS) - familjärt autoinflammatoriskt köldsyndrom (FCAS). Familjär medelhavsfeber (FMF) Kineret är avsett för behandling av familjär medelhavsfeber (FMF).
Kineret ska om lämpligt ges i kombination med kolkicin. Stills sjukdom: Kineret är avsett för vuxna, ungdomar, barn och spädbarn som är 8 månader och äldre med en kroppsvikt på 10 kg eller mer för behandling av Stills sjukdom, inklusive systemisk juvenil idiopatisk artrit (SJIA) och vuxendebuterande Stills sjukdom (AOSD), med aktiva systemiska manifestationer motsvarande måttlig till hög sjukdomsaktivitet eller för patienter med fortsatt sjukdomsaktivitet efter behandling med icke-steroida antiinflammatoriska läkemedel (NSAID) eller glukokortikoider. Kineret kan ges som monoterapi eller i kombination med andra antiinflammatoriska läkemedel och sjukdomsmodifierande antireumatiska läkemedel (DMARD).
Varningar och försiktighet: I kliniska studier har övergående förhöjningar av leverenzymer observerats. Vid användning efter godkännande för försäljning har hepatiska händelser som inte påverkar leverfunktionen rapporterats. Hepatiska händelser hos patienter med Stills sjukdom inträffar huvudsakligen under den första månaden av behandlingen med Kineret. Kineretbehandling bör inte påbörjas hos patienter med neutropeni
(antal neutrofila granulocyter <1,5 x 109/l). Behandling med Kineret ska inte påbörjas för patienter med aktiva infektioner. Med noggrann övervakning kan behandling med Kineret fortsätta även under en allvarlig infektion. Behandling med Kineret mot covid-19 kan fortsätta trots (sekundära) infektioner. Vid användning efter godkännande för försäljning har läkemedelsreaktion med eosinofili och systemiska symtom (DRESS) i sällsynta fall rapporterats hos patienter som behandlas med Kineret, framför allt hos pediatriska patienter med Stills sjukdom. Variera injektionsställe för att undvika tecken och reaktioner vid injektionsstället.
Förpackningar: 100 mg/0,67 ml injektionsvätska, lösning i en förfylld spruta, 7 förfyllda sprutor/förpackning. SPC uppdaterad september 2025.
För fullständig information vid förskrivning samt för priser se www.fass.se
Swedish Orphan Biovitrum AB, 112 76 Stockholm, telefon 08-697 20 00, www.sobi.se
PP-30283 10/2025
References
- Swedish Orphan Biovitrum AB (publ). Kineret summary of product characteristics [SmPC] 11/2024. Latest version available from: https://www.ema.europa.eu/en/documents/ product-information/kineret-epar-product-information_en.pdf
- Cavalli G, Dinarello CA. Anakinra therapy for non-cancer inflammatory diseases. Front Pharmacol. 2018; 9:1157
- Cavalli G, Colafrancesco S, Emmi G, et al. Interleukin 1α: a comprehensive review on the role of IL-1α in the pathogenesis and treatment of autoimmune and inflammatory diseases. Autoimmun Rev. 2021;20(3):102763
- van de Veerdonk, F.L., Netea, M.G. Blocking IL-1 to prevent respiratory failure in COVID-19. Crit Care 24, 445 (2020).