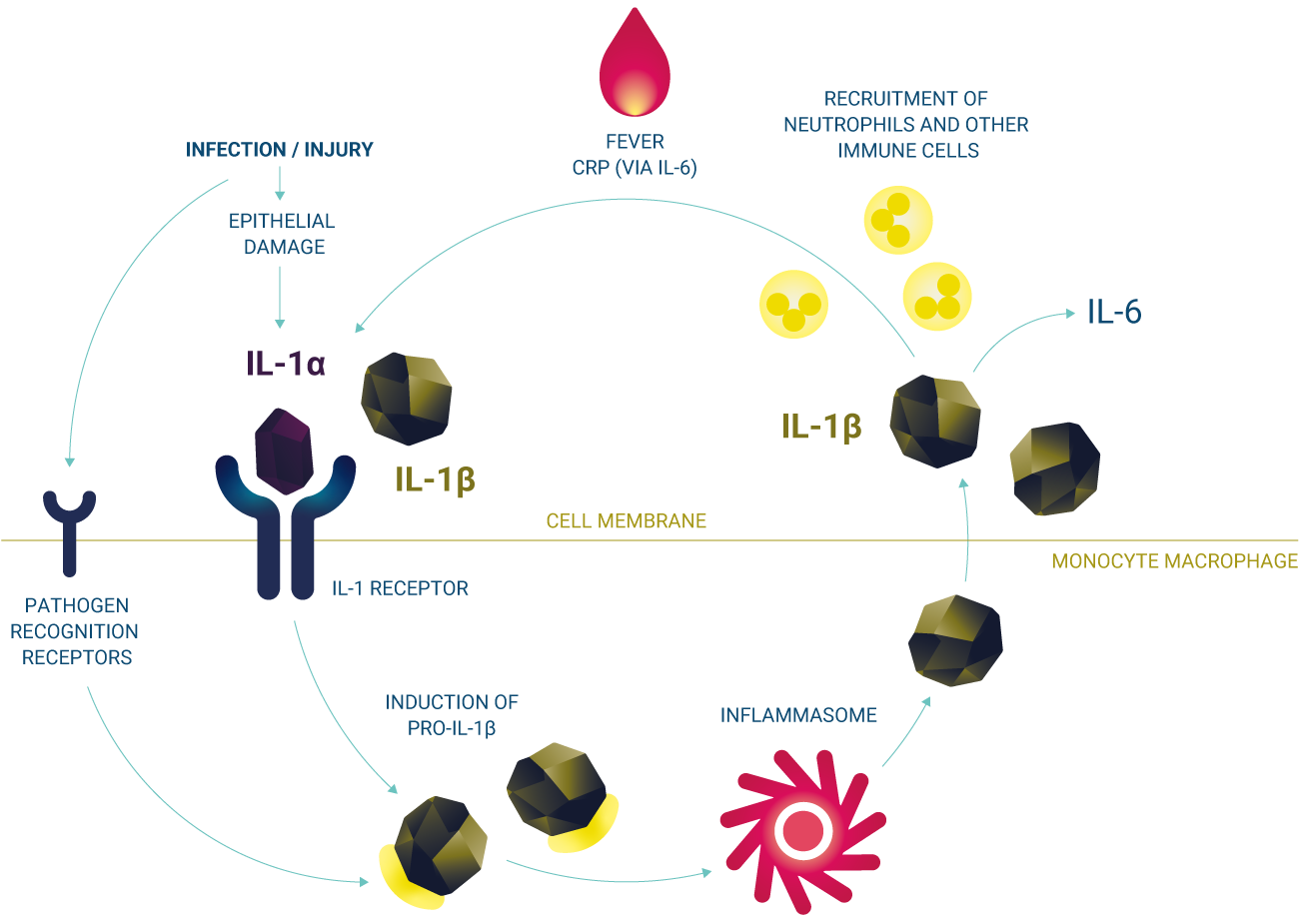
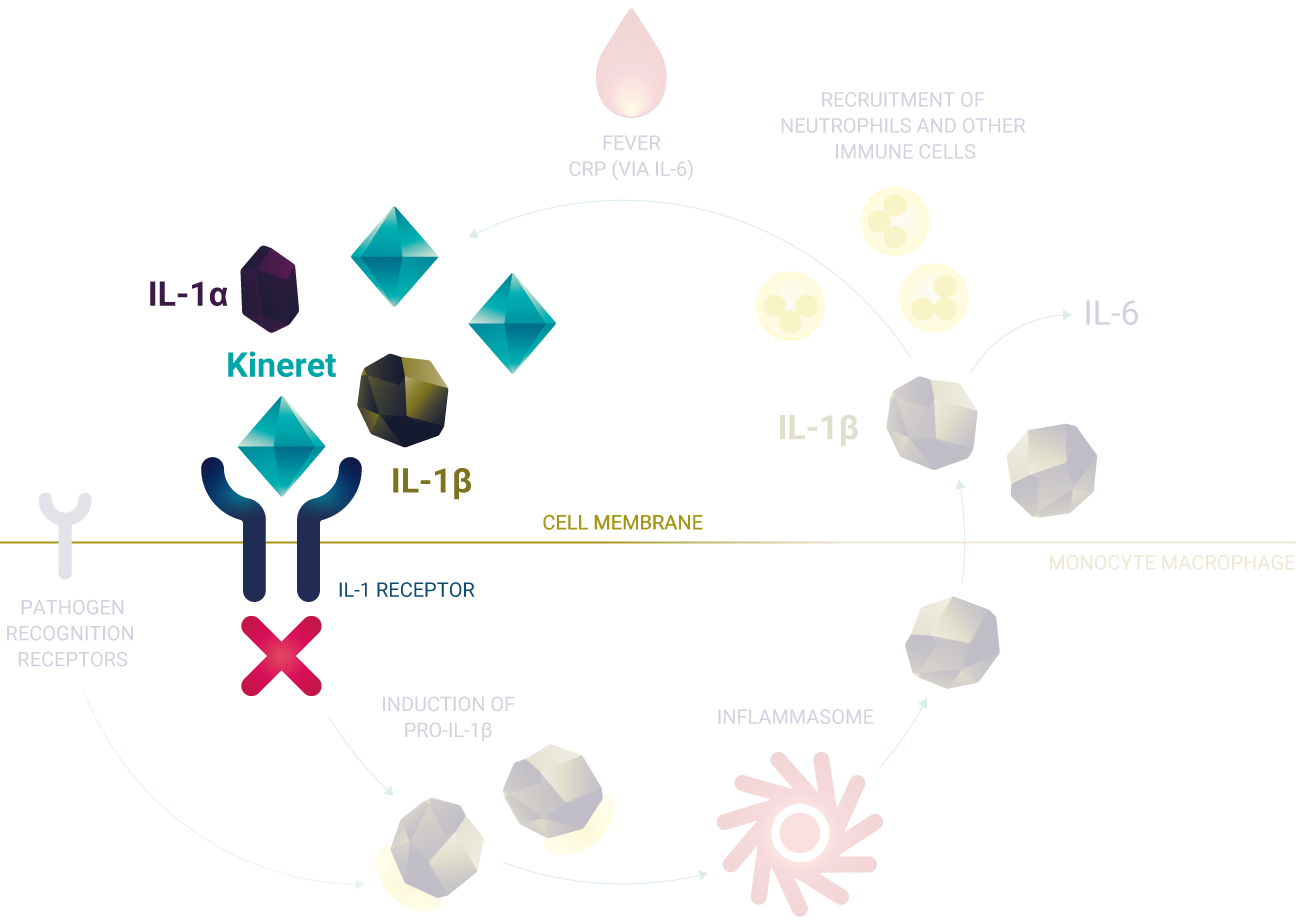
MODE OF ACTION
Kineret is a targeted treatment that neutralises the biological activity of both IL-1α and IL-1β1
Kineret is a recombinant version of the naturally occurring IL-1 receptor antagonist (IL-1Ra). Kineret acts by competitively inhibiting the biological activity of interleukin- 1α (IL-1α) and interleukin-1β (IL-1β), preventing both cytokines from attaching to the IL-1 receptor (IL-1R1) and initiating downstream signalling cascades.1,2 By blocking the interaction between IL-1α/IL-1β and IL-1R1, Kineret interrupts IL- 1-mediated inflammatory processes and alleviates the signs and symptoms of conditions characterised by excessive or dysregulated IL-1 responses.2
Approved indications for Kineret1
Rheumatoid Arthritis (RA) In adults for the treatment of the signs and symptoms of RA in combination with methotrexate, with an inadequate response to methotrexate alone.
COVID-19 Treatment of COVID-19 in adult patients with pneumonia requiring supplemental oxygen (low- or high-flow oxygen).
Cryopyrin-Associated Periodic Syndromes (CAPS) Neonatal-Onset Multisystem Inflammatory Disease (NOMID) / Chronic Infantile Neurological, Cutaneous, Articular Syndrome (CINCA) - Muckle-Wells Syndrome (MWS) and Familial Cold Autoinflammatory Syndrome (FCAS)
Familial Mediterranean Fever (FMF) Kineret should be given in combination with colchicine, if appropriate.
Still’s Disease Adults, adolescents, children and infants aged 8 months and older with a body weight of 10 kg or above for the treatment of Still’s disease, including Systemic Juvenile Idiopathic Arthritis (SJIA) and Adult-Onset Still’s Disease (AOSD).
See Kineret Prescribing information for summary of product characteristics for full prescribing and safety information
FAST ONSET
This is fast onset and short half life
Kineret has high absolute bioavailability after subcutaneous administration; maxi- mum plasma concentrations are reached within 3 to 7 hours and the terminal eli- mination half-life is 4 to 6 hours. Kineret induces a rapid resolution of systemic features such as fever, rash, and elevation of acute phase reactants.1
Safety
Please refer to current SmPC for more information about the safety and efficacy of Kineret.
For the full version of the Kineret SmPC in Danish, please click here
How is Kineret administered?
- Kineret is given in a pre-filled syringe containing 100 mg of anakinra per 0.67 ml (150 mg/ml).1
- Kineret is given once daily as a subcutaneous injection.1
- Dosage depends on indication. In children, the dose is determined depending on body weight. Please refer to current SmPC.
How should Kineret be stored?
- Kineret should be stored in a refrigerator between 2°C and 8°C.1
- Kineret should not be frozen or shaken.1
- Kineret should be kept in its original carton and away from light.1
Forkortet produktresumé for Kineret injektionsvæske
100 mg/0,67 ml, opløsning.
Indikationer: Reumatoid artrit (RA): Kineret®, i kombination med methotrexat, er indiceret til behandling af symptomer hos voksne med RA, som ikke responderer tilstrækkeligt på behandling med methotrexat alene. COVID-19: Kineret® er indiceret til behandling af sygdom med coronavirus 2019 (COVID-19) hos voksne patienter med lungebetændelse, hvor supplerende oxygen (med lavt eller højt flow) er påkrævet, og som er i risiko for at progrediere til svært respirationssvigt, bestemt ved plasmakoncentrationen af opløselig urokinase-plasminogenaktivator-receptor (suPAR) > 6 ng/ml. Kryopyrin-associerede periodiske syndromer (CAPS): Kineret® er indiceret til behandling af CAPS hos voksne, unge, børn og spædbørn i alderen 8 måneder og ældre, med en kropsvægt på 10 kilo eller derover, herunder:-neonatal multisystemisk inflammatorisk sygdom (NOMID)/kronisk infantilt neurologisk hud- og ledsyndrom (CINCA), - muckle-Wells syndrom (MWS) samt familiært auto-inflammatorisk kuldesyndrom (FCAS). Familiær middelhavsfeber (FMF): Kineret® er indiceret til behandling af familiær middelhavsfeber (FMF). Kineret® skal gives i kombination med colchicin, hvis relevant. Stills sygdom: Kineret® er indiceret til voksne, unge, børn og spædbørn i alderen 8 måneder og ældre med en kropsvægt på 10 kg eller derover til behandling af Stills sygdom, herunder systemisk juvenil idiopatisk artrit (SJIA) og Stills sygdom debuterende hos voksne (adult onset Still’s disease, AOSD), med aktive systemiske karakteristika af moderat til høj sygdomsaktivitet, eller hos patienter med vedvarende sygdomsaktivitet efter behandling med non- steroide anti-inflammatorika (NSAID’er) eller glukokortikoider. Kineret® kan gives som monoterapi eller i kombination med andre anti-inflammatorika og sygdomsmodificerende antireumatiske lægemidler (disease modifying antirheumatic drugs, DMARD’er). Dosering og administration*: Behandling med Kineret® bør påbegyndes og superviseres af en speciallæge med erfaring i diagnosticering og behandling af henholdsvis RA, COVID-19, CAPS, FMF og Stills sygdom. suPAR-testing: Hvis det er specificeret i indikationen, skal patient-udvælgelsen for behandlingen med Kineret® baseret på suPAR-niveau > 6 ng/ml måles med en valideret test. RA: Voksne: Den anbefalede dosis af Kineret® er 100 mg, som indgives én gang daglig ved subkutan injektion. Dosis bør indgives på cirka samme tidspunkt hver dag. COVID-19: Voksne: Den anbefalede dosis af Kineret® er 100 mg, som indgives én gang daglig ved subkutan injektion i 10 dage.CAPS: Voksne, unge, børn og spædbørn i alderen 8 måneder og ældre med en kropsvægt på 10 kilo eller derover. Startdosis: Den anbefalede startdosis til alle CAPS-undertyper er 1-2 mg/kg/dag ved subkutan injektion. Det terapeutiske respons afspejles primært i en reduktion af de kliniske symptomer som f.eks. feber, udslæt, ledsmerter og hovedpine, men også i de inflammatoriske serummarkører (CRP/SAA- niveauer) eller forekomst af opblussen. Vedligeholdelsesdosis ved mild CAPS (FCAS, mild MWS): Patienterne kan normalt kontrolleres tilfredsstillende ved at fastholde den anbefalede startdosis (1-2 mg/kg/dag). Vedligeholdelsesdosis ved alvorlig CAPS (MWS og NOMID/CINCA): Øgede doser kan være påkrævet inden for 1-2 måneder baseret på terapeutisk respons. Den normale vedligeholdelsesdosis ved alvorlig CAPS er 3-4 mg/kg/dag, som kan justeres til et maksimum på 8 mg/kg/dag. Ud over evalueringen af kliniske symptomer og inflammatoriske markører ved alvorlig CAPS, anbefales vurderinger af CNS- inflammation, herunder det indre øre (MR eller CT, lumbalpunktur og audiologi) og øjnene (oftalmologiske vurderinger) efter de første 3 måneders behandling og hver 6. måned derefter, indtil effektive behandlingsdoser er identificeret. Når patienter er klinisk velkontrolleret, kan CNS- og oftalmologisk monitorering udføres årligt. FMF: Den anbefalede dosis for patienter, der vejer 50 kg eller derover, er 100 mg/dag via subkutan injektion. Patienter, der vejer under 50 kg, skal doseres i henhold til kropsvægten, med en anbefalet dosis på 1-2 mg/kg/dag. Stills sygdom: Den anbefalede dosis for patienter, der vejer 50 kg eller derover, er 100 mg/dag via subkutan injektion. Patienter, der vejer under 50 kg, skal doseres i henhold til kropsvægten, med en startdosis på 1-2 mg/kg/dag. Responset på behandlingen skal evalueres efter 1 måned. I tilfælde af vedvarende systemiske manifestationer kan dosis justeres hos børn, eller den behandlende læge skal genoverveje en fortsat behandling med Kineret®. Ældre population (≥65 år): RA og COVID-19: Dosisjustering er ikke nødvendig. Dosering og administration er den samme dom for voksne mellem 18 og 64 år. CAPS og Stills sygdom: Der er begrænsede data hos ældre patienter. Der forventes ikke at være behov for dosisjusteringer. Pædiatrisk population (<18 år): Der foreligger ingen data hos børn under 8 måneder. RA: Kinerets® virkning hos børn med RA (JIA) i alderen 0 til 18 år er ikke klarlagt. COVID-19: Kinerets virkning hos børn med COVID-19 i alderen 0-18 år er ikke klarlagt. CAPS: Dosering og administration hos børn og spædbørn i alderen 8 måneder og ældre med en kropsvægt på 10 kilo eller derover er den samme som for voksne CAPS-patienter, baseret på kropsvægt. FMF: Børn, der vejer under 50 kg, doseres pr. kropsvægt, med en anbefalet dosis på 1-2 mg/kg/dag. Patienter, der vejer 50 kg eller der vejer 50 kg eller derover, doseres med 100 mg/dag. Hos børn med et utilstrækkeligt respons, kan dosis optrappes til 4 mg/kg/dag. Der er begrænsede data for virkning af Kineret hos børn under 2 år med FMF. Stills sygdom: Børn, der vejer under 50 kg, doseres pr. kg. kropsvægt, med en startdosis på 1-2 mg/kg/dag. Patienter, der vejer 50 kg eller derover, doseres med 100 mg/dag. Hos børn med et utilstrækkeligt respons, kan dosis optrappes til 4 mg/kg/dag. Kineret® skal anvendes med forsigtighed ved nedsat lever og nyrefunktion, og for korrekt dosering i forbindelse hermed henvises til punkt 4.2 i produktresumeet. Administration: Kineret® indgives ved subkutan injektion. Kineret® leveres klar til brug i en gradueret fyldt injektionssprøjte, som gør det muligt at give doser fra 20 til 100 mg. Sprøjten er derfor ikke egnet til børn med en kropsvægt på under 10 kg.
Kontraindikationer: Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne eller over for proteiner fra E. coli. Behandling med Kineret® må ikke igangsættes i tilfælde af patienter med neutropeni (ANC <1,5 x 109/l). Særlige advarsler og forsigtighedsregler vedrørende brugen*: Allergiske reaktioner: De fleste allergiske reaktioner er makulopapuløse eller urtikarielle udslæt. Hvis en alvorlig allergisk reaktion forekommer, skal Kineret® seponeres og passende behandling initieres. Leverrelaterede hændelser: I kliniske studier er der set forbigående forhøjelser af leverenzymer. Disse forhøjelser har ikke kunnet associeres til tegn eller symptomer på hepatocellulære skader, undtagen hos én patient med SJIA, der udviklede alvorlig hepatitis i forbindelse med en infektion med cytomegalovirus. Leverhændelser hos patienter med Stills sygdom forekommer hovedsageligt i løbet af den første måned af behandling med Kineret®. Rutinemæssig kontrol af leverenzymer i løbet af den første måned bør overvejes, især hvis patienten har prædisponerende faktorer, eller udvikler symptomer, der indikerer leverdysfunktion. Alvorlige infektioner: Forøget hyppighed af alvorlige infektioner relaterede sig hovedsageligt til luftvejene. Kineret®-behandling må ikke iværksættes i tilfælde af patienter med aktive infektioner. Kineret®-behandling skal seponeres hos RA-patienter, hvis der udvikles en alvorlig infektion. Hos Kineret®-behandlede CAPS- eller FMF-patienter er der risiko for sygdomsopblussen, når Kineret®-behandlingen seponeres. Med nøje overvågning kan behandlingen med Kineret® fortsættes, selv under en alvorlig infektion. Behandlingen af COVID-19 med Kineret® kan fortsættes trods (sekundære) infektioner. Læger bør udvise forsigtighed ved administration af Kineret® til patienter, som har haft gentagne infektioner, eller som har en anden sygdom, som bevirker, at de er udsatte for at få infektioner. Patienten skal screenes for latent tuberkulose før iværksættelse af behandlingen med Kineret®, og der skal også tages højde for de gældende medicinske retningslinjer. Desuden skal der også udføres screening for viral hepatitis i henhold til offentliggjorte retningslinjer før igangsættelse af behandling med Kineret®. Nedsat nyrefunktion: Kineret® elimineres ved glomerulær filtration og efterfølgende tubulær metabolisme. Som følge heraf falder plasmaclearance af Kineret® med en nedsat nyrefunktion. Dosisjustering er ikke nødvendig for patienter med let nedsat nyrefunktion (kreatininclearance (CLcr) 60 til 89 ml/ minut). Kineret® bør anvendes med forsigtighed hos patienter med moderat nedsat nyrefunktion (CLcr 30 til 59 ml/minut). Hos patienter med svært nedsat nyrefunktion (CLcr <30 ml/minut) eller nyresygdom i slutstadiet, herunder dialyse, bør det overvejes at administrere den ordinerede dosis af Kineret® hver anden dag. Neutropeni: Behandling med Kineret® bør ikke påbegyndes hos patienter med neutropeni (ANC <1,5 x 109/l). Det skal anbefales, at de neutrofile optællinger bliver foretaget inden behandling med Kineret® påbegyndes, og når behandling med Kineret® er i gang, månedligt de første 6 måneder og derefter kvartalsvist. Hos de patienter, som bliver neutropeniske (ANC <1,5 x 109/l), bør ANC kontrolleres tæt, og behandling med Kineret® seponeres. Kinerets® sikkerhed og virkning hos patienter med neutropeni er ikke blevet evalueret. Lungehændelser: Der er indberettet hændelser af interstitiel lungesygdom, pulmonal alveolær proteinose og lungehypertension, primært hos pædiatriske patienter med Stills sygdom behandlet med IL-6- og IL-1-hæmmere, herunder Kineret. Det ser ud som om, at patienter med trisomi 21 er overrepræsenteret. Et kausalt forhold til Kineret er ikke klarlagt.
Medikamentelt udslæt med eosinofili og systemiske symptomer (DRESS): Der er i sjældne tilfælde rapporteret om medikamentelt udslæt med eosinofili og systemiske symptomer (DRESS) hos patienter i behandling med Kineret ved anvendelse efter markedsføringen, fortrinsvis hos pædiatriske patienter med STILLs sygdom (systemisk juvenil idiopatisk artritis (SJIA). Det kan være nødvendigt at indlægge patienter med DRESS, da denne tilstand kan have dødelig udgang. Hvis der observeres tegn og symptomer på DRESS, og der ikke kan etableres en anden ætiologi, bør Kineret seponeres, og en anden behandling overvejes.
Amyloidose (systemisk): Hos patienter med NOMID/CINCA som fik høje doser Kineret over længere tid og havde amyloidaflejringer på injektionsstedet (se pkt. 4.8), er der rapporteret isolerede tilfælde af systemisk AIL1RAP (IL-1-receptorantagonistprotein)-amyloidose efter markedsføring. Hos patienter med bekræftede amyloidaflejringer på injektionsstedet anbefales observation for symptomer på systemisk amyloidose, herunder nøje overvågning for proteinuri.
Immunsuppression: Virkningen af behandling med Kineret® hos patienter med eksisterende malignitet er ikke blevet undersøgt. Derfor kan det ikke anbefales at anvende Kineret® hos patienter med eksisterende malignitet. Maligniteter: RA-patienter kan have større risiko (gennemsnitligt 2-3 gange) for at udvikle lymfom. Kliniske forsøg har vist, at forekomsten svarer til de hyppigheder, der generelt rapporteres hos RA-patienter. I kliniske forsøg var hyppigheden af malignitet den samme hos de Kineret-behandlede og de placebobehandlede patienter, og den var ikke forskellig fra forekomsten i baggrundspopulationen. Endvidere er den generelle hyppighed af malignitet ikke øget i de 3 år, hvor patienter har modtaget behandling med Kineret. Vaccinationer: I et placebokontrolleret klinisk forsøg (n = 126) blev der ikke registreret forskel i anti-tetanus antistofrespons mellem grupper behandlet med Kineret® og grupper behandlet med placebo, når en tetanus/difteri toxoid- vaccine blev administreret sammen med Kineret®. Der er ikke tilgængelige data over effekten af vaccination med andre inaktiverede antigener, eller COVID-19 vacciner, hos patienter, der behandles med Kineret®. Der er ikke tilgængelige data vedrørende effekten af levende vaccine eller den sekundære transmission af infektion ved levende vacciner hos patienter, der behandles med Kineret®. Derfor bør levende vaccine ikke gives sammen med Kineret®. Ældre population (≥65 år): Sammenlagt deltog 752 RA-patienter ≥65 år, inklusive 163 patienter ≥75 år og 173 COVID-19-patienter ≥65 år, i de kliniske studier. Samlet var der ingen forskel i sikkerhed og effektivitet observeret mellem disse patienter og de yngre patienter. Der er begrænset erfaring med behandling af ældre patienter med CAPS, FMF og Stills sygdom. Fordi der generelt er en højere hyppighed af infektioner hos den ældre population, bør der udvises særlig forsigtighed ved behandling af ældre patienter.
COVID-19-patienter: Virkningen af behandlingen med Kineret® er ikke klarlagt hos COVID-19-patienter med suPAR < 6 ng/ml. Behandlingen med Kineret® bør ikke iværksættes hos patienter, der har behov for ikke-invasiv eller invasiv mekanisk ventilering eller ekstrakorporal membranoxygenering (ECMO), da virkningen ikke er klarlagt hos disse patientpopulationer.
Interaktion med andre lægemidler og andre former for interaktion*: Samtidig brug af Kineret® og etanercept eller andre TNFα-antagonister kan ikke anbefales. Cytochrom P450-substrater: Dannelsen af CYP450-enzymer undertrykkes af de forhøjede niveauer af cytokiner (f.eks. IL-1) under kronisk inflammation. I tilfælde af en IL-1-antagonist som anakinra kunne det således forventes, at dannelsen af CYP450-enzymet skulle kunne normaliseres under behandling. Dette ville være klinisk relevant for CYP450-substratet med et smalt terapeutisk indeks (f.eks. warfarin og phenytoin). Ved påbegyndelse eller afslutning af Kineret®-behandling af patienter, der er i behandling med disse typer af lægemidler, kan det være relevant at overveje terapeutisk monitorering af disse produkters virkning eller koncentration, lige som det kan være nødvendigt at justere den individuelle dosis af lægemidlet. Fertilitet, graviditet og amning*: For en sikkerheds skyld bør Kineret® undgås under graviditeten og til kvinder i den fertile alder, som ikke anvender sikker kontraception. Amning skal ophøre under behandling med Kineret®.
Bivirkninger*: Der er ingen indikationer på, at den samlede sikkerhedsprofil hos patienter med CAPS, FMF eller Stills sygdom er forskellig fra profilen hos patienter med RA, med undtagelse af observation efter markedsføring af en højere frekvens af indberettede leverhændelser hos patienter med Stills sygdom.Den samlede sikkerhedsprofil hos patienter med COVID-19, der blev behandlet med Kineret®, svarer til sikkerhedsprofilen for Kineret-behandlede patienter med RA. Meget almindelige bivirkninger: Hovedpine, reaktioner på injektionsstedet og forhøjet kolesterol. Almindelige bivirkninger: Alvorlige infektioner, neutropeni og trombocytopeni. Ikke almindelige bivirkninger: Forhøjede leverenzymer, udslæt og allergiske reaktioner, herunder anafylaktiske reaktioner, angioødem, urticaria og pruritus.
Amyloidaflejringer på injektionsstedet
Ved brug efter markedsføring er der blevet indberettet enkelte tilfælde af amyloidaflejringer på injektionsstedet hos patienter med NOMID/CINCA, som fik høje doser af Kineret injiceret subkutant i det samme hudområde over lange perioder. Det anbefales derfor at skifte mellem injektionsstederne. For nærmere beskrivelse af ovennævnte bivirkninger samt immunogenicitet og leverhændelser henvises til punkt 4.8 i produktresumeet.
Medikamentelt udslæt med eosinofili og systemiske symptomer (DRESS)
Der er i sjældne tilfælde rapporteret om medikamentelt udslæt med eosinofili og systemiske symptomer (DRESS) hos patienter i behandling med Kineret ved anvendelse efter markedsføringen, fortrinsvis hos pædiatriske patienter med Stills sygdom [systemisk juvenil idiopatisk artritis (SJIA)]. Se pkt. 4.4. i produktresuméet.
Overdosering: Ingen dosisbegrænsende toksiciteter blev observeret i kliniske studier. I undersøgelser af sepsis modtog 1.015 patienter Kineret® i doser på op til 2 mg/kg/time i.v. (~35 gange den anbefalede dosis til RA) over en 72 timers behandlingsperiode. Profilen af uønskede hændelser i disse studier viser ingen forskel fra det, som er fundet i undersøgelser hos patienter med reumatoid artrit. Særlige opbevaringsforhold: Opbevares i køleskab (2 °C ‑ 8 °C). Må ikke nedfryses. Opbevares i den originale pakning for at beskytte mod lys. Ved ambulant anvendelse kan Kineret opbevares ved stuetemperatur op til 25 °C i maks. 72 timer. Efter Kineret tages ud af køleskabet, skal det anvendes i løbet af 72 timer eller bortskaffes. Efter opbevaring ved stuetemperatur må Kineret ikke sættes tilbage i køleskabet.
Pakninger og priser: Injektionsvæske 100 mg/0,67 ml, opløsning i fyldt injektionssprøjte: 7 stk. Dagsaktuel pris kan findes på www.medicinpriser.dk. Tilskud: Ej tilskud. Udlevering: BEGR. Indehaver af markedsføringstilladelsen: Swedish Orphan Biovitrum AB (publ), SE 112 76 Stockholm, Sverige. Lokal kontakt: Sobi A/S, Sorgenfrivej 17, 2800 Lyngby, tlf.: 32966869
De med * markerede afsnit er forkortet i forhold til det godkendte produktresumé. Produktresumeet kan vederlagsfrit rekvireres hos Sobi A/S, Sorgenfrivej 17, 2800 Lyngby, tlf.: 32966869 eller ses på www.ema.europa.eu
REF-18411 Oktober 2025
References
- Swedish Orphan Biovitrum AB (publ). Kineret summary of product characteristics [SmPC] 11/2024. Latest version available from: https://www.ema.europa.eu/en/documents/ product-information/kineret-epar-product-information_en.pdf
- Cavalli G, Dinarello CA. Anakinra therapy for non-cancer inflammatory diseases. Front Pharmacol. 2018; 9:1157
- Cavalli G, Colafrancesco S, Emmi G, et al. Interleukin 1α: a comprehensive review on the role of IL-1α in the pathogenesis and treatment of autoimmune and inflammatory diseases. Autoimmun Rev. 2021;20(3):102763
- van de Veerdonk, F.L., Netea, M.G. Blocking IL-1 to prevent respiratory failure in COVID-19. Crit Care 24, 445 (2020).